Аутор:
Lewis Jackson
Датум Стварања:
5 Може 2021
Ажурирати Датум:
1 Јули 2024

Садржај
Мол је стандардна мерна јединица у хемији, која се користи за гледање различитих елемената у једињењу. Обично се маса једињења израчунава у грамима (г) и треба је претворити у моларне јединице. Прелазак је прилично једноставан, међутим, још увек постоје неки важни кораци које морамо следити. Користећи доњу методу, лако можете претворити граме у молове.
Кораци
Део 1 од 2: Израчунати молекулску масу
Припремите потребне залихе за решавање математичког задатка. Када имате на располагању све алате, биће лакше решити проблем. Оно што вам треба је:
- Оловка и папир. Математика постаје лакша када све запишете на папир. Морате представити све кораке да бисте постигли максималан резултат.
- Периодни систем хемијских елемената: користи се за одређивање атома масе елемената.
- Џепни калкулатор: користи се за израчунавање компликованих бројева.

Одредите које елементе у једињењу требате претворити у моларне јединице. Први корак у израчунавању молекуларне масе је одређивање елемената који чине једињење. То је лако јер је скраћеница елемената само један до два знака.- Ако је супстанца скраћена са два знака, прво слово је написано великим, а друго слово малим словом. Пример: Мг је скраћеница за елемент магнезијум.
- Једињења НаХЦО3 састоји се од четири елемента: натријум (На), водоник (Х), угљеник (Ц) и кисеоник (О).
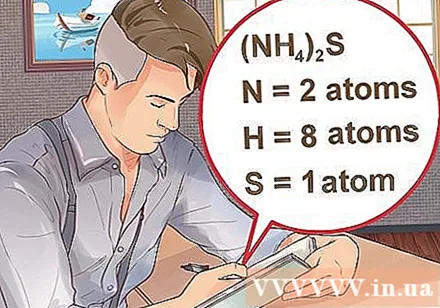
Одреди број атома за сваки елемент у једињењу. Морате знати атомски број сваке супстанце у једињењу да бисте израчунали молекул масе тог једињења. Мали број поред скраћенице елемента представља атомски број елемента.- Пример: једињење Х.2О има два атома водоника и један атом кисеоника.
- Ако је једињење написано у заградама, попраћено малим индексом, то значи да сваки састојак у заградама множи индекс. Пример: једињење (НХ4)2С се састоји од два Н атома, осам Х атома и једног С атома.

Запишите кубни атомски папир за сваки елемент. Коришћење периодног система је најлакши начин за проналажење кубног атома елемента. Након што лоцирате елемент на периодном систему, видећете атомску масу одмах испод иконе елемента.- На пример, кубни атом кисеоника је 15,99.
Израчунати молекулску масу. Молекул масе супстанце једнак је броју атома сваког елемента помноженом са масним атомом тог елемента. Ова количина је битна у конверзији у грам у молар.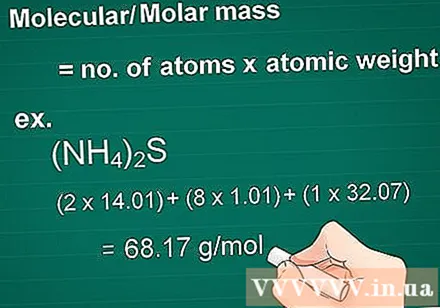
- Прво помножите атомски број сваког елемента у једињењу са његовим масним атомом.
- Затим заједно додајте масе елемената у једињењу.
- Пример: Молекулска маса једињења (НХ4)2С = (2 к 14,01) + (8 к 1,01) + (1 к 32,07) = 68,17 г / мол.
- Молекуларна маса је такође позната и као моларна маса.
Део 2 од 2: Претворите граме у мол
Подесите формулу за конверзију. Да бисте пронашли број молова једињења, поделите број грама једињења са моларном масом тог једињења.
- Формула: број молова = маса (грами) / моларна маса једињења (грам / мол)
Замените бројеве у формулу. Након подешавања праве формуле, следећи корак је замена бројева које сте израчунали у формулу. Ако желите да се уверите да су подаци у исправном положају, можете их проверити потискивањем јединице. Ако су након једноставности преостала јединица мадежи, онда сте правилно постављени.
Реши једначину. Помоћу калкулатора поделите масу са кубним молекулом супстанце или једињења. Количник ће бити број молова супстанце или једињења које тражите.
- На пример, проблем је са 2 г воде (Х2О) и тражи од вас да га претворите у моларне јединице. Имамо моларну масу Х.2О је 18г / мол. Поделите 2 са 18, тако да имате 0,1111 мол Х2О.
Савет
- Не заборавите да уз одговоре наведете име елемента или сложенице.
- Ако се од вас затражи да представите вежбу или квиз, обавезно јасно покажите своје одговоре кружењем или цртањем оквира око одговора.
Шта вам је потребно
- Хемијски периодни систем
- Оловка
- Папир
- рачунар
- Проблеми са хемијом