Аутор:
Judy Howell
Датум Стварања:
27 Јули 2021
Ажурирати Датум:
23 Јуни 2024

Садржај
- На корак
- 1. део од 4: Разумевање структуре
- 2. део од 4: Разумевање симбола и именовања
- Део 3 од 4: Очитавање атомског броја
- Део 4 од 4: Очитавање атомске масе
Периодни систем елемената је списак од 118 елемената који су до сада откривени. Постоји неколико симбола и бројева који указују на разлике у елементима, док структура табеле организује елементе према сличностима. Периодни систем можете прочитати користећи доленаведене смернице.
На корак
1. део од 4: Разумевање структуре
 Периодичну таблицу сматрајте као да започиње у горњем левом углу и завршава се на крају последњег реда, доњег и десног. Табела је структурисана слева надесно по редоследу све већег атомског броја. Атомски број је број протона у једном атому.
Периодичну таблицу сматрајте као да започиње у горњем левом углу и завршава се на крају последњег реда, доњег и десног. Табела је структурисана слева надесно по редоследу све већег атомског броја. Атомски број је број протона у једном атому. - Нису сваки ред или колона комплетни. Иако у средини могу бити празнине, наставите читати табелу с лева на десно. На пример, водоник има атомски број 1 и налази се у горњем левом углу. Хелијум има атомски број 2 и налази се у горњем десном углу.
- Елементи од 57 до 71 обично су приказани као подскуп у доњем десном углу табеле. То су „ретки земаљски елементи“.
 У свакој колони табеле наћи ћете „групу“ елемената. Постоји 18 колона.
У свакој колони табеле наћи ћете „групу“ елемената. Постоји 18 колона. - Користите термин „читање групе“ за читање од врха до дна.
- Нумерисање је обично назначено изнад колона; међутим, може бити и под другим групама, попут метала.
- Нумерација која се користи у периодном систему се веома разликује. Могу бити римски (ИА), арапски (1А) или бројеви од 1 до 18.
- Водоник може бити из породице халогена и алкалних метала, или обоје.
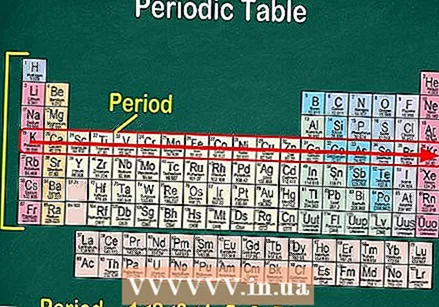 У сваком реду табеле наћи ћете „тачке“ елемената. Постоји 7 периода. Користите фразу „читај дуж тачке“ за читање слева надесно.
У сваком реду табеле наћи ћете „тачке“ елемената. Постоји 7 периода. Користите фразу „читај дуж тачке“ за читање слева надесно. - Периоди су обично нумерисани од 1 до 7 на левој страни табеле.
- Сваки период је већи од претходног. Ово је повезано са повећањем нивоа енергије атома у периодном систему.
 Разумевање додатних група уз метал, полуметал и неметал. Боје се веома разликују.
Разумевање додатних група уз метал, полуметал и неметал. Боје се веома разликују. - Група Метали имају једну боју. Међутим, водоник често има исту боју и групу као и неметали. Метали имају сјај, обично су чврсти на собној температури, проводе топлоту и електричну енергију, а савитљиви су и савитљиви.
- Неметали имају исту боју. То су елементи од Ц-6 до Рн-86, укључујући Х-1 (водоник). Немају сјај, проводе топлоту и електричну енергију и нису податни. Они обично формирају гас на собној температури и могу бити чврста супстанца, гас или течност.
- Полу-метали / металоиди обично имају љубичасту или зелену боју, као комбинацију друге две боје. Линија је дијагонална и протеже се од елемената Б-5 до Ат-85. Имају нека својства метала, а нека неметала.
 Имајте на уму да су елементи понекад наведени и у породицама. То су алкални метали (1А), земноалкалијски метали (2А), халогени (7А), племенити гасови (8А) и атоми угљеника (4А).
Имајте на уму да су елементи понекад наведени и у породицама. То су алкални метали (1А), земноалкалијски метали (2А), халогени (7А), племенити гасови (8А) и атоми угљеника (4А). - Бројеви могу бити римски, арапски или стандардни бројеви.
2. део од 4: Разумевање симбола и именовања
 Прво прочитајте симбол. Састоји се од једног или два слова и стандардан је на неколико језика.
Прво прочитајте симбол. Састоји се од једног или два слова и стандардан је на неколико језика. - Симбол се може извести из латинског назива елемента или његове заједничке заједничке ознаке.
- У многим случајевима, симбол следи енглеску конвенцију о именовању, као што је Хелиум или "Хе". Међутим, није правило које можете претпоставити. На пример, гвожђе је „Фе“. Из тог разлога се комбинација симбола / имена обично памти за брзу употребу.
 Погледајте заједничко име. Ово је директно испод симбола. Ово се разликује у зависности од језика на којем је написан периодни систем.
Погледајте заједничко име. Ово је директно испод симбола. Ово се разликује у зависности од језика на којем је написан периодни систем.
Део 3 од 4: Очитавање атомског броја
 Прочитајте периодни систем према атомском броју у горњем центру оквира сваког елемента. Као што је раније поменуто, систем је распоређен од горе лево доле десно. Познавање атомског броја је најбржи начин да потражите више информација о елементу.
Прочитајте периодни систем према атомском броју у горњем центру оквира сваког елемента. Као што је раније поменуто, систем је распоређен од горе лево доле десно. Познавање атомског броја је најбржи начин да потражите више информација о елементу. 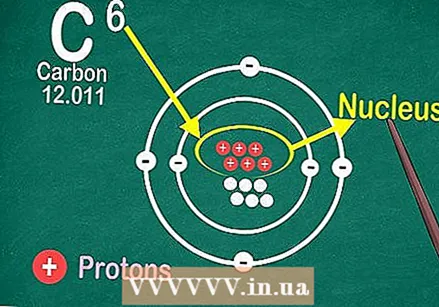 Атомски број је број протона у језгру појединог атома елемента.
Атомски број је број протона у језгру појединог атома елемента. Додавањем или уклањањем протона ствара се другачији елемент.
Додавањем или уклањањем протона ствара се другачији елемент. Проналажење броја протона у атому такође одређује број електрона. Атоми имају толико електрона колико и протона.
Проналажење броја протона у атому такође одређује број електрона. Атоми имају толико електрона колико и протона. - Имајте на уму да од овог правила постоји изузетак. Када атом изгуби или добије електроне, он постаје електрички наелектрисани јон.
- Ако се поред симбола елемента налази знак плус, то значи да је позитивно наелектрисан. Симболом минус је негативно наелектрисан.
- Ако не постоји симбол плус или минус, а ваш хемијски проблем није у вези са јонима, онда је број протона и електрона вероватно једнак.
Део 4 од 4: Очитавање атомске масе
 Одредити атомску масу. Ово је број испод уобичајеног назива елемента.
Одредити атомску масу. Ово је број испод уобичајеног назива елемента. - Иако се може чинити да се атомска маса повећава од левог горњег дела система до доњег десног, то није тачно у свим случајевима.
 Схватите да је већина елемената представљена децималним местима. Атомска маса је збир честица у језгру; међутим, то је пондерисани просек различитих изотопа.
Схватите да је већина елемената представљена децималним местима. Атомска маса је збир честица у језгру; међутим, то је пондерисани просек различитих изотопа.  Помоћу атомске масе пронађите број неутрона у једном атому. Заокружите атомску масу на најближи цели број, масени број. Затим од масеног броја одузмете број протона да бисте одредили број неутрона.
Помоћу атомске масе пронађите број неутрона у једном атому. Заокружите атомску масу на најближи цели број, масени број. Затим од масеног броја одузмете број протона да бисте одредили број неутрона. - На пример: Атомска маса гвожђа је 55,847, па је његов масени број 56. Елемент има 26 протона. 56 (масени број) минус 26 (протони) је 30. У једном атому гвожђа обично има 30 неутрона.
- Промена броја неутрона у атому ствара изотопе, који су тежа или лакша верзија атома.



