Аутор:
Bobbie Johnson
Датум Стварања:
10 Април 2021
Ажурирати Датум:
1 Јули 2024

Садржај
- Кораци
- 1. део од 2: Припремите опрему
- 2. део од 2: Спроведите експеримент
- Савјети
- Упозорења
- Шта ти треба
Процес цепања воде (Х.2О) у своје саставне делове (водоник и кисеоник) помоћу електричне енергије назива се електролиза. Гасови добијени као резултат електролизе могу се сами користити - на пример, водоник служи као један од најчишћих извора енергије. Иако назив овог процеса може звучати помало паметно, заправо је лакше него што би могло изгледати ако имате одговарајућу опрему, знање и мало искуства.
Кораци
1. део од 2: Припремите опрему
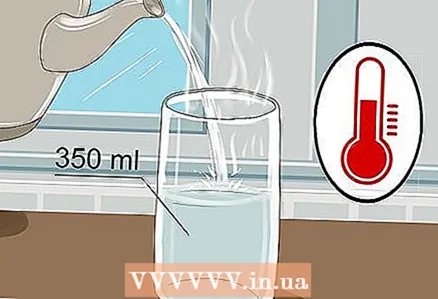 1 Узмите чашу од 350 мл и сипајте у њу топлу воду. Нема потребе да чашу пуните до врха, довољно је само мало воде. Хладна вода ће бити довољна, иако топла вода боље проводи струју.
1 Узмите чашу од 350 мл и сипајте у њу топлу воду. Нема потребе да чашу пуните до врха, довољно је само мало воде. Хладна вода ће бити довољна, иако топла вода боље проводи струју. - Вода из чесме и флаширана вода ће бити довољни.
- Топла вода има мањи вискозитет, што олакшава кретање јона.
 2 Растопите 1 кашику (20 грама) кухињске соли у води. Сипајте со у чашу и промешајте воду да се раствори. Ово ће створити слани раствор.
2 Растопите 1 кашику (20 грама) кухињске соли у води. Сипајте со у чашу и промешајте воду да се раствори. Ово ће створити слани раствор. - Натријум хлорид (тј. Кухињска со) је електролит који повећава електричну проводљивост воде. Сама по себи, вода не проводи добро електричну енергију.
- Након што повећате електричну проводљивост воде, струја коју ствара батерија лакше ће проћи кроз раствор и ефикасније разградити молекуле на водоник и кисеоник.
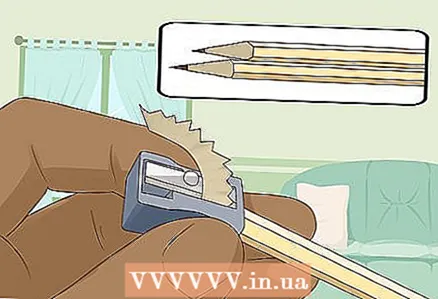 3 Оштрите две тврде меке оловке на оба краја да бисте открили оловку. Не заборавите да уклоните гумицу са оловака. Графитна шипка треба да стрши на оба краја.
3 Оштрите две тврде меке оловке на оба краја да бисте открили оловку. Не заборавите да уклоните гумицу са оловака. Графитна шипка треба да стрши на оба краја. - Графитне шипке ће служити као изолиране електроде на које прикључујете батерију.
- Графит је добро погодан за овај експеримент јер се не отапа нити кородира у води.
 4 Изрежите лист картона довољно велик да се положи на стакло. Употријебите прилично дебели комад картона који неће попустити након што у њему избушите двије рупе. Изрежите квадратни комад из кутије за ципеле или слично.
4 Изрежите лист картона довољно велик да се положи на стакло. Употријебите прилично дебели комад картона који неће попустити након што у њему избушите двије рупе. Изрежите квадратни комад из кутије за ципеле или слично. - Картон се користи за држање оловака у води тако да не додирују странице и дно стакла.
- Картон није проводљив, па га можете безбедно ставити на стакло.
 5 Оловкама избушите две рупе у картону. Картон пробушите оловкама - у овом случају они ће бити чврсто стегнути и неће клизити. Пазите да графит не додирује странице или дно стакла, иначе ће ометати експеримент.
5 Оловкама избушите две рупе у картону. Картон пробушите оловкама - у овом случају они ће бити чврсто стегнути и неће клизити. Пазите да графит не додирује странице или дно стакла, иначе ће ометати експеримент.
2. део од 2: Спроведите експеримент
 1 Повежите једну жицу са алигаторским копчама на сваки прикључак батерије. Батерија ће служити као извор електричне струје, а кроз жице са стезаљкама и графитним шипкама струја ће допирати до воде.Спојите једну жицу са стезаљком на позитивну, а другу на негативни пол батерије.
1 Повежите једну жицу са алигаторским копчама на сваки прикључак батерије. Батерија ће служити као извор електричне струје, а кроз жице са стезаљкама и графитним шипкама струја ће допирати до воде.Спојите једну жицу са стезаљком на позитивну, а другу на негативни пол батерије. - Користите батерију од 6 волти. Ако га немате, можете користити батерију од 9 волти.
- Одговарајућу батерију можете набавити у продавници електричне енергије или супермаркету.
 2 Повежите друге крајеве жица са оловкама. Чврсто причврстите стезаљке од металне жице на графитне шипке. Можда ћете морати да одлепите још мало дрвета са оловака како квачице не би склизнуле са графитних шипки.
2 Повежите друге крајеве жица са оловкама. Чврсто причврстите стезаљке од металне жице на графитне шипке. Можда ћете морати да одлепите још мало дрвета са оловака како квачице не би склизнуле са графитних шипки. - Тако ћете затворити круг, а струја из батерије ће тећи кроз воду.
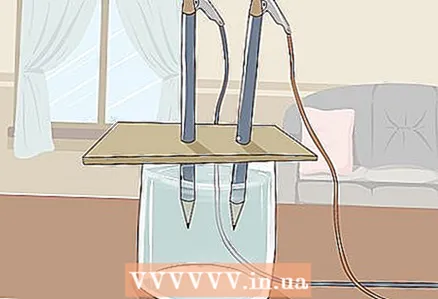 3 Поставите картон на стакло тако да слободни крајеви оловака буду потопљени у воду. Лист картона треба да буде довољно велик да стане на стакло. Пазите да не ометате правилно постављање оловака.
3 Поставите картон на стакло тако да слободни крајеви оловака буду потопљени у воду. Лист картона треба да буде довољно велик да стане на стакло. Пазите да не ометате правилно постављање оловака. - Да би експеримент био успешан, графит не сме да додирује зидове и дно стакла. Проверите ово поново и по потреби подесите оловке.
 4 Гледајте како се вода дели на водоник и кисеоник. Мехурићи гаса ће почети да се подижу из графитних шипки уроњених у воду. То су водоник и кисеоник. Водоник ће се ослобађати на негативном полу, а кисеоник на позитивном полу.
4 Гледајте како се вода дели на водоник и кисеоник. Мехурићи гаса ће почети да се подижу из графитних шипки уроњених у воду. То су водоник и кисеоник. Водоник ће се ослобађати на негативном полу, а кисеоник на позитивном полу. - Чим спојите жице на батерију и графитне шипке, електрична струја ће тећи кроз воду.
- На оловци која је повезана са негативним полом формираће се више мехурића гаса, јер се сваки молекул воде састоји од два атома водоника и једног атома кисеоника.
Савјети
- Ако немате оловке са графитним вратилом, уместо њих можете користити две мале жице. Само омотајте један крај сваке жице око одговарајућег ступа батерије, а други умочите у воду. Резултат ће бити исти као и код оловака.
- Покушајте да користите другу батерију. Количина струје која тече зависи од напона батерије, што заузврат утиче на брзину цепања молекула воде.
Упозорења
- Ако у воду додате електролит, попут соли, имајте на уму да ће експеримент генерисати малу количину нуспроизвода, као што је хлор. У тако малим количинама је сигуран, али можете осетити благи мирис хлора.
- Изведите овај експеримент под надзором одраслих. Повезан је са електричном енергијом и гасовима и стога може бити опасан, иако мало вероватан.
Шта ти треба
- Две тврде меке оловке
- Једна батерија од 6 или 9 волти
- Стакло запремине 350 милилитара
- 2 жице са крокодилским копчама
- Оштрач за оловку
- Со