Аутор:
Randy Alexander
Датум Стварања:
2 Април 2021
Ажурирати Датум:
1 Јули 2024

Садржај
Хемијска једначина је симболички приказ хемијске реакције. Реагенси су написани на левој страни, а производ на десној страни. Закон очувања масе указује да се ниједан атом не рађа или губи у хемијској реакцији, па број атома присутних у реактанту мора бити једнак броју атома присутних у реакцији. производа. Следећи овај водич, можете уравнотежити хемијске једначине на различите начине.
Кораци
Метод 1 од 2: Равнотежа према традиционалној методи
Напиши дату једначину. У овом примеру бисте имали: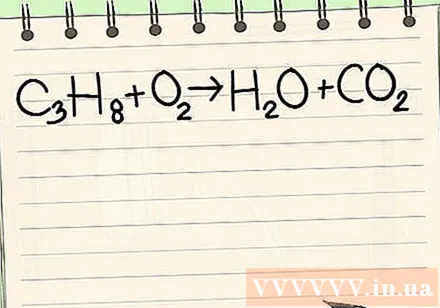
- Ц.3Х.8 + О.2 -> Х.2О + ЦО2
- Ова реакција се јавља када пропан (Ц.3Х.8сагорева у кисеонику да би се створила вода и угљен-диоксид.

Запишите број атома за сваки елемент који имате на свакој страни једначине. Погледајте индексе испод сваког атома да бисте пронашли број атома у једначини.- Лево: 3 угљеника, 8 водоника и 2 кисеоника.
- Десно: 1 угљеник, 2 водоника и 3 кисеоника.
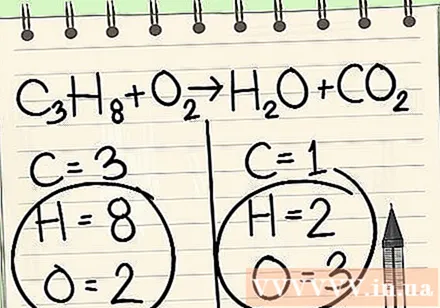
На крају увек оставите водоник и кисеоник.
Ако вам је остало више од једног елемента за равнотежу: Изаберите елемент који се појављује само у једном молекулу реактанта и само у појединачном молекулу производа. То значи да ћете прво морати да уравнотежите атоме угљеника.
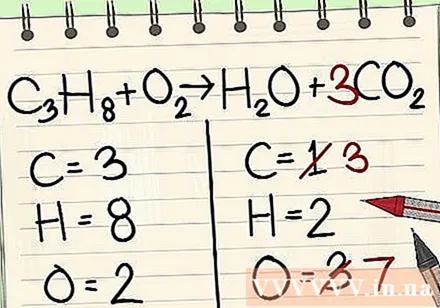
Додајте коефицијент за појединачне атоме угљеника на десну страну једначине да бисте је уравнотежили са три атома угљеника на левој страни једначине.- Ц.3Х.8 + О.2 -> Х.2О + 3ЦО2
- Фактор 3 испред угљеника на десној страни указује да постоје 3 атома угљеника, баш као што индекс испод 3 на левој страни означава 3 атома угљеника.
- У хемијској једначини можете променити коефицијент, али не и индекс.
Следећа је атомска равнотежа водоника. Са леве стране имате 8 атома водоника. Отуда ће вам требати 8 на десној страни.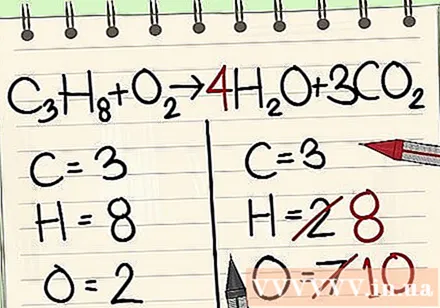
- Ц.3Х.8 + О.2 -> 4Х2О + 3ЦО2
- Десно од сата додајете 4 као фактор јер доњи број показује да већ имате 2 атома водоника.
- Када помножите фактор 4 са индексом 2, добијате 8.
- Осталих 6 атома кисеоника су из 3ЦО2. (3к2 = 6 атома кисеоника + 4 остала атома кисеоника = 10)
Уравнотежите атоме кисеоника.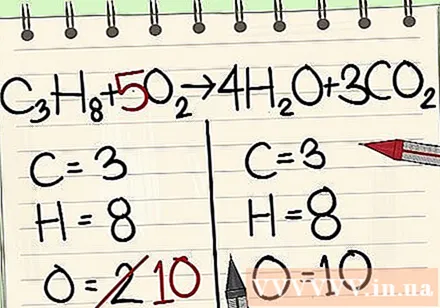
- Пошто сте молекулима десно од једначине додали коефицијенте, број атома кисеоника се променио. Сада имате 4 атома кисеоника у молекулу воде и 6 атома кисеоника у молекулу угљен-диоксида. Укупно имамо 10 атома кисеоника.
- Додајте фактор 5 молекулу кисеоника лево од једначине. Сада на свакој страни имате по 10 молекула кисеоника.
- Ц.3Х.8 + 5О2 -> 4Х2О + 3ЦО2.

- Атоми угљеника, водоника и кисеоника су у равнотежи. Ваша једначина је завршена.
Метод 2 од 2: Равнотежа према алгебарској методи
Напиши једначине према симболима и формулама. Пример а = 1 и на основу те формуле напиши једначину.
Замените цифре њиховим променљивим.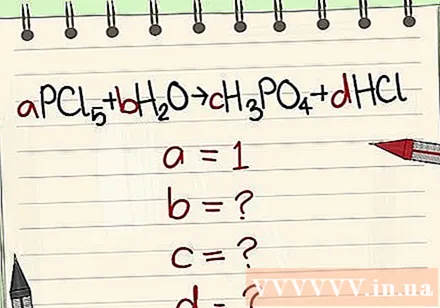
Проверите количину елемената у реактору као и страну производа.
- Пример: аПЦл5 + бХ2О = цХ3ПО4 + дХЦл тако да је а = 1 б = ц = д = и раздвајање елемената П, Цл, Х, О, тако да добијате а = 1 б = 4 ц = 1 д = 5 .
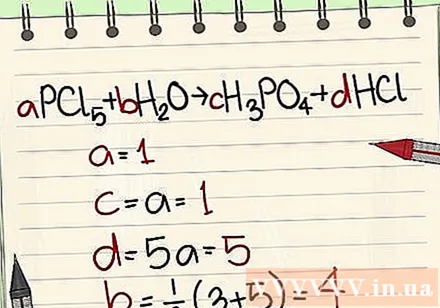
- Пример: аПЦл5 + бХ2О = цХ3ПО4 + дХЦл тако да је а = 1 б = ц = д = и раздвајање елемената П, Цл, Х, О, тако да добијате а = 1 б = 4 ц = 1 д = 5 .
Савет
- Не заборавите да поједноставите једначину.
- Ако имате проблема, можете да унесете једначину у алатку за равнотежу на мрежи да бисте је уравнотежили. Имајте на уму да када полажете испит немате приступ мрежном билансу, па немојте зависити од њега.
Упозорење
- Никада не користите коефицијент као удео у хемијској једначини - у хемијској реакцији не можете поделити молекуле или атоме.
- Током процеса равнотеже можете користити разломке, али једначина неће бити уравнотежена ако су коефицијенти и даље разломци.
- Да бисте уклонили разломке, помножите целу једначину (леву и десну) са именитељем разломка.